2023. 07
CBL-514 用於非手術局部減脂之 CBL-0205 Phase 2b 臨床試驗申請已獲美國 FDA 核准執行
2023 年 7 月 31 日- 康霈生技(6919-TW)新藥 CBL-514 注射劑用於非手術局部減脂(減少皮下脂肪)之 CBL-0205 Phase 2b 臨床試驗申請,已於今日獲美國食品藥物管理局(U.S. FDA)核准執行。
本試驗案為一項多國多中心、隨機分配、安慰劑組對照的 Phase 2b 臨床試驗,將招募中度或重度腹部皮下脂肪堆積( Grade 3 (moderate) or Grade 4 (severe) using the Abdominal Fat Rating Scale (AFRS))的受試者,預計納入 160 位受試者,並於 2023 年 Q4 於美國和加拿大多個中心開始收案,惟實際時程將依執行進度調整。本公司後續將繼續進行加拿大臨床試驗申請與試驗收案之相關準備工作。
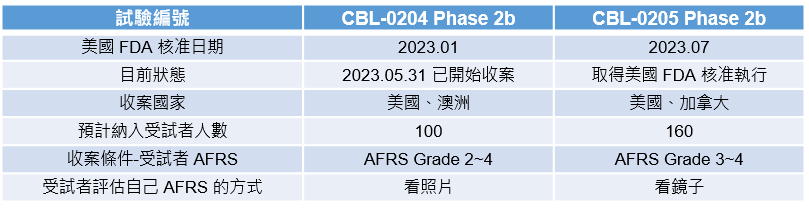
本試驗案與 CBL-514 目前正在美國與澳洲進行收案的 CBL-0204 Phase 2b 臨床試驗,皆為遵從美國 FDA 建議所執行的 Phase 2b 臨床試驗,CBL-514 非手術局部減脂二個 Phase 2b 試驗的設計類似,主要差異如下:
根據 Deloitte 中國身體塑形市場行業發展白皮書指出,中國局部減脂市場在 2020 年超過 15 億美元,在 2030 年將成長至 154 億美元,推估全球市局部減脂市場將超過 1,025 億美元。根據 2022 年 ASPS 報告,抽脂手術是美國最受歡迎的美容手術,顯示局部減脂龐大的市場需求。目前局部減脂 75-80% 採用侵入性的外科手術,包含抽脂手術與腹部整形術,雖然療效較目前已上市非手術局部減脂產品明顯許多,但術後恢復期長且具有嚴重副作用與後遺症,手術風險高。目前非手術局部減脂產品包括冷凍減脂(Cryolipolysis)、超音波減脂、局部減脂注射劑(成分為去氧膽酸或其鹽類)等,雖然副作用較外科手術低,但療效不佳無法明顯減少治療部位皮下脂肪,且術後需 12 週以上才能看到療效,並且仍然具有中重度副作用,也有包含組織壞死、神經受損、面癱、纖維化疤痕組織、硬塊、反常脂肪增生 (paradoxical adipose hyperplasia, PAH) 、皮膚灼燒或潰瘍...等嚴重副作用之風險。美國整型醫學會報告指出,目前仍有超過 60% 的人因為不滿意現行的治療方式或害怕副作用而卻步,顯示局部減脂市場仍有大量未被滿足的醫療需求。
本試驗案為一項多國多中心、隨機分配、安慰劑組對照的 Phase 2b 臨床試驗,將招募中度或重度腹部皮下脂肪堆積( Grade 3 (moderate) or Grade 4 (severe) using the Abdominal Fat Rating Scale (AFRS))的受試者,預計納入 160 位受試者,並於 2023 年 Q4 於美國和加拿大多個中心開始收案,惟實際時程將依執行進度調整。本公司後續將繼續進行加拿大臨床試驗申請與試驗收案之相關準備工作。
本試驗案與 CBL-514 目前正在美國與澳洲進行收案的 CBL-0204 Phase 2b 臨床試驗,皆為遵從美國 FDA 建議所執行的 Phase 2b 臨床試驗,CBL-514 非手術局部減脂二個 Phase 2b 試驗的設計類似,主要差異如下:

根據 Deloitte 中國身體塑形市場行業發展白皮書指出,中國局部減脂市場在 2020 年超過 15 億美元,在 2030 年將成長至 154 億美元,推估全球市局部減脂市場將超過 1,025 億美元。根據 2022 年 ASPS 報告,抽脂手術是美國最受歡迎的美容手術,顯示局部減脂龐大的市場需求。目前局部減脂 75-80% 採用侵入性的外科手術,包含抽脂手術與腹部整形術,雖然療效較目前已上市非手術局部減脂產品明顯許多,但術後恢復期長且具有嚴重副作用與後遺症,手術風險高。目前非手術局部減脂產品包括冷凍減脂(Cryolipolysis)、超音波減脂、局部減脂注射劑(成分為去氧膽酸或其鹽類)等,雖然副作用較外科手術低,但療效不佳無法明顯減少治療部位皮下脂肪,且術後需 12 週以上才能看到療效,並且仍然具有中重度副作用,也有包含組織壞死、神經受損、面癱、纖維化疤痕組織、硬塊、反常脂肪增生 (paradoxical adipose hyperplasia, PAH) 、皮膚灼燒或潰瘍...等嚴重副作用之風險。美國整型醫學會報告指出,目前仍有超過 60% 的人因為不滿意現行的治療方式或害怕副作用而卻步,顯示局部減脂市場仍有大量未被滿足的醫療需求。


